TEST DI UTILITÀ CLINICA SECONDARIA
HOME – DIAGNOSI FERTILITÀ – FEMMINILE

Test di utilità clinica secondaria
Post Coital Test
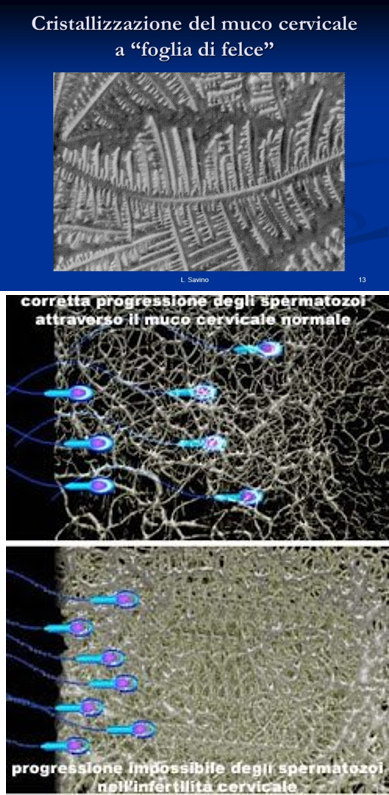
- Consente studiare le proprietà del muco cervicale nel periodo ovulatorio e apprezzare la mobilità degli spermatozoi all’interno del muco stesso.
- La raccolta del muco è indolore, priva di rischi e non necessita ricovero ospedaliero
- La raccolta va eseguita a distanza di 6-12 ore dal rapporto sessuale
- Consiste nell’aspirazione del muco endocervicale che viene esaminato al microscopio per verificare:
- Abbondanza,
- Viscosità,
- Trasparenza
- Ph
- Modo di cristalizzazione
- La presenza di spermatozoi mobili annotando il tipo di mobilità.
Interpretazione
-
- Test positivo – muco abbondante, filante, buona cristalizzazione (a foglia di falce che indica buona estrogenizzazione), PH compreso tra 6.5 – 8.5, presenza nel campo visivo di almeno 5 spermatozoi con motilità progressiva rettilinea veloce
- Test negativo con buona qualità del muco – presenza nel campo visivo di pochi spermatozoi con scarsa motilità (motilità in situ con movimento oscillante) oppure immobili.
- Test negativo con scarsa qualità del muco – muco poco abbondante, PH acido, opaco, scarsa cristalizzazione, pochi spermatozoi mobili.
Utilità
- Un PCT negativo indica il fattore cervicale di infertilità
- In tal caso è indicato indagare sulla presenza di anticorpi anti- spermatozoo
- Nonostante sia stato utilizzato per decenni PCT non è mai stato standardizzato, pertanto la sua interpretazione è operatore dipendente
- Diversi studi hanno dimostrato che la predittività del test sia bassa
- Uno studio randomizzato ha dimostrato che l’utilizzo del test conduca all’esecuzione di altri test e trattamenti aspecifici che non incrementano la possibilità di gravidanza bensì comportano una perdita di tempo prezioso alla coppia.
- La Società Americana di Riproduzione Assistita (ASRM) è del parere che l’esecuzione di PCT abbia poco razionale clinico.
Don’t perform a postcoital test (PCT) for the evaluation of infertility, ASRM, 2013.
Temperatura basale
- La temperatura basale TB è la temperatura corporea che si registra in condizioni basali, cioè al momento del risveglio, prima di iniziare qualunque attività.
- L’importanza di tale misurazione si basa sul fatto che essa varia a seconda della fase del ciclo mestruale in relazione alla variazione della concentrazione sierica del progesterone.
- TB subisce un incremento pari a 0.1-03 °C durante la fase luteinica in seguito all’incremento del progesterone circolante
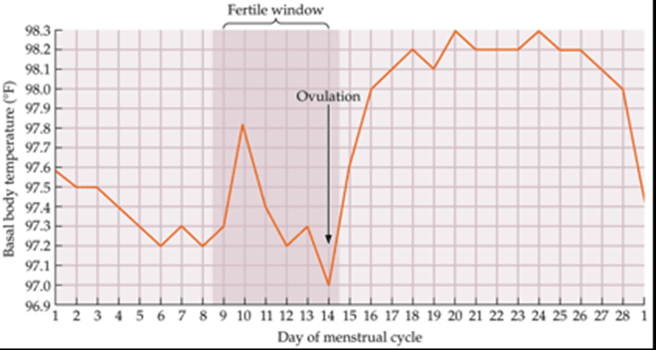
- In un ciclo ovulatorio la temperatura assumerà un andamento cosiddetto “bifasico” – bassa nella fase follicolare, seguita da un incremento dopo 2 giorni dal picco di LH e persistente per tutta la fase luteinica.
Vantaggi
- TB è una metodica semplice e poco costosa per la diagnosi di ovulazione
Svantaggi
- TB non predice il periodo fertile, in quanto l’ovulazione si verifica prima dell’incremento della temperatura
- Ha un utilizzo retrospettivo per dimostrare l’avvenuta ovulazione
- Spesso è di difficile interpretazione
- Alcune donne ovulano presentando una TB monofasica
- TB non è indicatore sensibile della funzione del corpo luteo cioè NON è in grado di diagnosticare l’insufficienza del corpo luteo
Evaluation of female infertility, Wendy Kuohung, MD, Mark D Hornstein, MD
Up to date, 2019
Biopsia endometriale e valutazione della fase luteale
- L’ovulazione implica la produzione di progesterone con trasformazione secretiva dell’endometrio e la biopsia endometriale lo può dimostrare
- Il test va eseguito nella fase medio-luteale del ciclo mestruale
- Questa tipologia di esame è stata a lungo considerata «gold standard» nella valutazione della funzione luteale e la diagnosi di insufficienza del corpo luteo.
- Studi più approfonditi hanno dimostrato che la biopsia endometriale per valutare l’inadeguatezza della funzione luteale non sia un metodo diagnostico valido per la mancanza di precisione e accuratezza e soprattutto non può distinguere le donne fertili da quelle infertili
- Perciò la biopsia endometriale non è più indicata per la valutazione della funzione ovulatoria o luteale nelle pazienti infertili e dovrebbe essere limitata solo ai casi di patologia endometriale sospetta (es. neoplasie, endometrite cronica)
Don’t perform endometrial biopsy in the routine evaluation of infertility. ASRM, 2015
Biopsia endometriale e recettività endometriale
- Endometrial Receptivity Array – ERA Test è una nuova procedura diagnostica che aiuta a determinare se la cavità endometriale è pronta all’impianto embrionario
- Consiste nel prelevare un campione di endometrio per l’analisi molecolare di 236 geni correlati allo stato di recettività endometriale
- Il test svela ulteriori informazioni sulla «finestra di impianto» – periodo di maggior recettività endometriale durante il ciclo mestruale della donna e che ha durata di 4-5 gg
- ERA test – NON è un esame di routine nell’iter diagnostico di infertilità femminile
- È indicato nelle pazienti con ripetuti fallimenti di impianto embrionario (RIF) oppure nei casi di poliabortività
ERA Test
-
- È una procedura ambulatoriale, non richiede anestesia
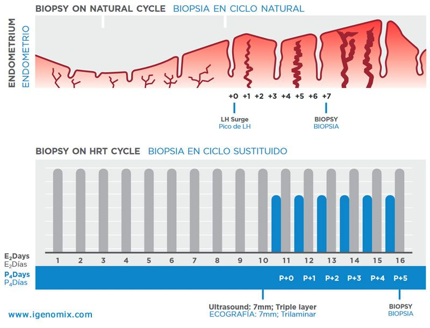
- Può essere eseguito in cicli naturali o di terapia ormonale sostitutiva, secondo il tipo di ciclo in cui verrà eseguito successivamente il trasferimento embrionario
- Consiste nel prelevare un campione di endometrio dal fondo uterino utilizzando un catetere Pipelle
- La biopsia va eseguita quando si pensa che si verifichi la finestra di impianto e dovrebbe corrispondere al giorno del presunto trasferimento embrionario
Interpretazione
- Ricettivo: Il profilo di espressione genica coincide con quello di un endometrio ricettivo normale.
- Pre-ricettivo: Il profilo di espressione genica coincide con quello di un endometrio in fase pre-ricettiva. Può essere dovuto allo spostamento della finestra di impianto e, per confermarlo, occorre analizzare una seconda biopsia nel giorno raccomandato.
- Post-ricettivo: Il profilo di espressione genica coincide con quello di un endometrio in fase post-ricettiva. Può essere dovuto allo spostamento della finestra di impianto e, per confermarlo, occorre analizzare una seconda biopsia nel giorno raccomandato.
La diagnosi di ricettività è valida per il tipo di ciclo in cui si è eseguito il test e pertanto l’embrione deve essere trasferito nello stesso tipo di ciclo e nella finestra di impianto personalizzata entro cui è stata ottenuta una diagnosi “ricettiva”.
Endometriocoltura
La cavita’ uterina non e’ sterile:
- In condizioni normali la specie colonizzante più presente è il Lactobacillus (>90%) che agisce come probiotico, in grado di inibire la crescita di batteri, virus e funghi
- La presenza di batteri patogeni (es. Stafilococco, Streptococco, Enterococco, Ureaplasma, Mycoplasma, Escherichia, Klebsiella, Neisseria e Chlamydia) può essere causa di infezioni, fallimento di impianto embrionario o aborto.
- Il più importante esempio di patologia causata dall’infezione della mucosa endometriale da parte dei germi patogeni è l’Endometrite Cronica (CE)
- CE è spesso asintomatica
- Attualmente la diagnosi si basa su istologia, isteroscopia e/0 coltura microbica
- L’endometriocoltura è l’attuale metodo «gold standard» per la valutazione delle infezioni batteriche MA
- E’ stato dimostrato che il 20-60 % dei batteri non possono essere coltivati
- La microbiologia molecolare cioè la valutazione dei genomi dei microorganismi (microbioma endometriale) consente la rilevazione dei batteri coltivabili e non coltivabili
Screening del microbioma endometriale – Endometriome
- Endometriome – test di screening eseguito mediante la tecnologia di sequenziamento del DNA (NGS) su campione di tessuto endometriale
- Permette di identificare la presenza di più di 10 batteri patogeni responsabili di endometrite cronica
- Permette di valutare la percentuale di Lactobacillus nel microbiota endometriale
- Nel caso in cui il test suggerisca una disbiosi o presenza di patogeni è possibile proporre un trattamento correttivo o una cura antibiotica appropriata
Indicazioni
- È indicato nelle pazienti con ripetuti fallimenti di impianto
- Poliabortività
- Sospetta endometrite cronica
NON è un esame di routine nell’iter diagnostico di infertilità femminile.
Interpretazione
Risultato negativo:
- il microbioma endometriale è normale (Lactobacillus come specie dominante >90%)
Risultato positivo:
- Presenza di batteri che causano disbiosi o di batteri patogeni
- Lattobacillus < 90%
- Patogeni rilevati correlati a sviluppo di endometrite cronica o malattie sessualmente trasmissibili
- Fortemente correlato a fallimento di impianto o rischio aumentato di aborto
Screening immunologico
Diversi studi hanno investigato sul ruolo dei fattori autoimmuni nell’impianto embrionario in pazienti infertili. I più comuni anticorpi studiati sono stati:
- Ab antifosfolipidi,
- Ab antitiroidei (anti TPO, antiTG)
- Ab Antinucleo (ANA),
- Ab antigliadina,
- Ab antiovarici ,
- Ab antispermatozoo
Sebbene sia stata dimostrata un’associazione tra gli anticorpi antifosfolipidi e la poliabortività, secondo gli studiosi una valutazione di routine nella donna infertile dei fattori autoimmuni non è indicata
MA
Si ritiene opportuna la loro valutazione nei casi di ripetuti fallimenti delle tecniche di PMA
Immune testing in fertility practice: truth or deception? Kallen CB, Curr Opin Obstet Gynecol. 2003
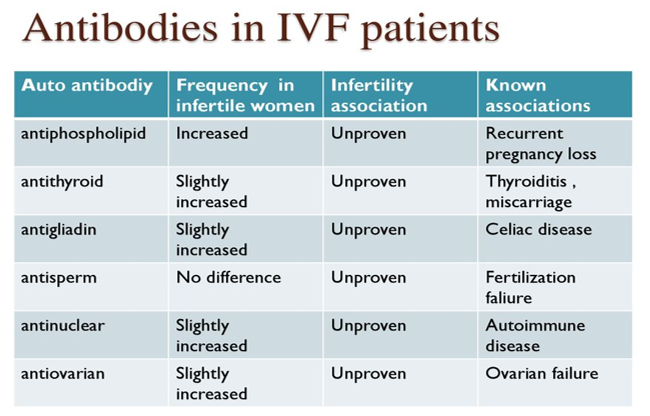
Ruolo degli anticorpi nelle pazienti infertili sottoposte a PMA
Immunological screening in women undergoing IVF, D.M. Butawan, W.H Kutteh, How to improve your ART success rates, Cambridge 2011
Screening genetico
- 8-10% delle infertilità femminili sono causate o associate ad alterazioni genetiche
- Includono alterazioni cromosomiche o mutazioni di singoli geni
- Alterazioni numeriche o strutturali del cariotipo possono rispettivamente provocare amenorrea, menopausa precoce o un elevato rischio di aborti ripetuti.
- Le linee guida suggeriscono eseguire il cariotipo a tutte le donne infertili con disfunzione ovarica primaria o poliabortività
- Il cariotipo è obbligatorio nelle donne candidate a tecniche di PMA
- Varie mutazioni monogeniche, come ad esempio la talassemia o la sindrome dell’X-fragile, possono ridurre la capacità riproduttiva.
Linee guida per la diagnosi genetica della coppia infertile, C. Foresta, 2011

Conclusioni diagnostiche della donna infertile
Alla fine del percorso diagnostico le donne infertili vengono suddivise nelle seguenti categorie:
- Donne con sterilità assoluta:
- Tubarica (salpingectomia od occlusione tubarica bilaterale)
- Ovulatoria – menopausa precoce (da POF, annessectomia bilaterale, terapie gonadotossiche) oppure ipogonadismo ipogonadotropo
- Uterina – isterectomia oppure agenesia utero-vaginale
- Donne con infertilità inspiegata – dove l’iter diagnostico non è stato in grado di mettere in evidenza alcuna alterazione degli organi riproduttivi;
- Donne sub-fertili, dove la funzionalità degli organi riproduttivi risulta compromessa, ma non assente;
- Donne con abortività ricorrente, cioè con tre o più episodi di aborto spontaneo (circa il 5%).

